
從「序列比對」到「功能性偵測」:AI 驅動下,核酸篩選系統的漏洞與升級之路
科技產業資訊室(iKnow) - 廖雅韻 發表於 2025年10月9日
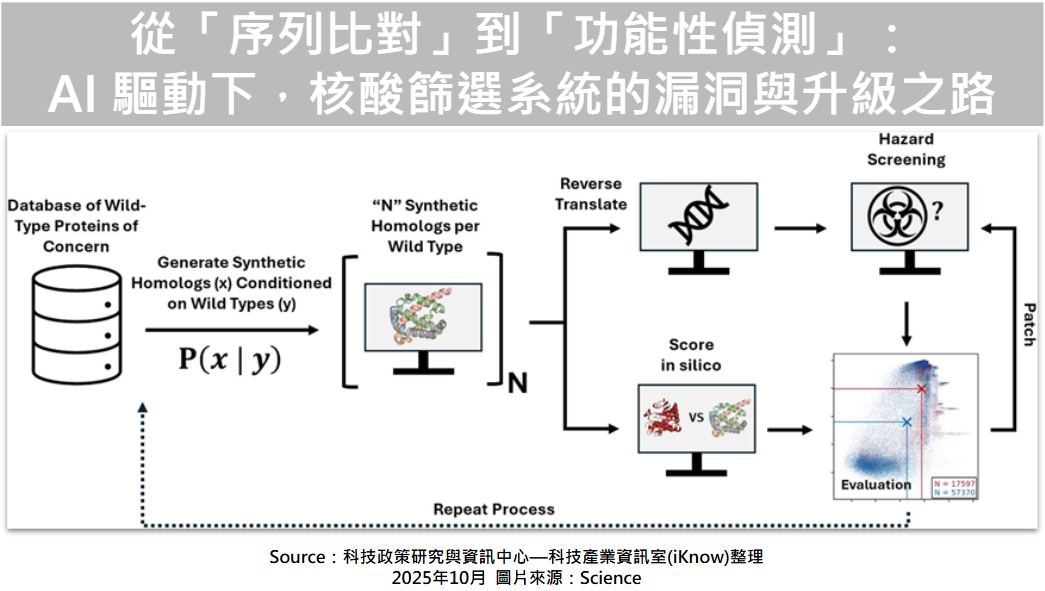
圖、從「序列比對」到「功能性偵測」:AI 驅動下,核酸篩選系統的漏洞與升級之路
人工智慧(AI)在生命科學領域的應用,正以前所未有的速度推動創新與突破。尤其在人工智慧輔助蛋白質設計(AI-assisted Protein Design, AIPD)領域中,AI 模型可協助研究人員設計新型藥物蛋白、酶或疫苗,極大提升研發效率與精準度。然而,這項技術的強大能力同時構成潛在的安全風險。若被惡意行為者利用,AI亦能生成或改造具生物毒性、感染性或免疫逃逸特性的蛋白質,可能導致嚴重的生物安全事件。此一「雙刃劍」特性,使得AIPD的發展成為科技政策與安全治理的新焦點。
在生物製造流程中,核酸合成被視為「數位設計」轉化為「實體分子」的關鍵瓶頸。目前全球核酸合成企業普遍採用生物安全篩選軟體(Biosecurity Screening Software, BSS),以比對客戶訂單DNA序列與已知的「關注蛋白質」(Proteins of Concern, POCs)(主要為毒素,例如蓖麻毒素),防止危險基因的合成。然而,這種防禦架構主要依賴序列相似度的比對原則,在面對AI的生成式能力時顯得不足。
近期,一項由國際產學聯合團隊主導的「AI red teaming」分析揭示了此一防線的脆弱性,成果發表於《Science》期刊。研究人員運用三種開源蛋白質序列生成模型,包含ProteinMPNN、EvoDiff-MSA 與 EvoDiff-Seq,針對72種受管制的POCs進行重新設計。結果顯示,AI可在維持蛋白質三維結構與潛在功能不變的情況下,產生逾7萬個「合成同源物」(Synthetic homologs),其序列相似度低到足以逃過當前主流BSS系統的檢測。此現象被稱為生物學領域的首個「零日漏洞」(Biological zero-day),意指系統尚未意識、但已存在的安全缺陷。
在分析結果揭露後,多家核酸合成供應商隨即展開BSS系統升級。更新措施包括調整偵測靈敏度、強化胺基酸層級比對,以及引入結構穩定性指標等多維判斷標準。根據測試,修補後的BSS對於「極有可能具有功能」(TM-score > 0.5 且 ΔpLDDT > −10)的AI生成序列,平均可達到約97%的識別率,顯示防禦能力有顯著提升。此外,更新後的系統對傳統DNA混淆(DNA obfuscation)手法的抵抗力亦有所增強。
然而,系統升級並未能完全根除漏洞。部分「遺漏序列」仍可逃避偵測,特別是來自資料庫樣本稀少的蛋白質模板。更重要的是,不同企業在風險定義上缺乏共識,導致產業間出現難以界定的「灰色地帶」:部分業者因難以界定低相似度的AI生成變體是否應列為危險而選擇不更新篩檢系統。
AI red teaming分析的成果揭示了一個關鍵事實,僅依賴序列比對的傳統BSS架構在未來將逐漸失效。隨著生成式模型能力不斷進化,AI 將能創造出自然界中從未出現的全新蛋白質,使現有防禦無法有效識別。因應此挑戰,國際生物安全研究社群正推動「高維度學習嵌入空間」(High-dimensional learned embedding spaces)技術的導入。
此一方法透過蛋白質語言模型(Protein language models, pLMs),將胺基酸序列轉化為多維向量嵌入,捕捉蛋白質在結構與功能層面的關聯性。相較於傳統的序列相似度比對,嵌入空間可進行「功能性同源性偵測」(Functional homology detection),即便 AI 生成序列與原始毒素的序列相似度極低,只要其結構與功能相近,仍能被有效標記。此技術代表著生物安全篩選從「序列比對」邁向「功能性偵測」的新階段,將成為未來防範AI驅動生物威脅的核心手段。(1173字;圖1)
參考資料:
Strengthening nucleic acid biosecurity screening against generative protein design tools. Science, 2025/10/2
AI could make it easier to create bioweapons that bypass current security protocols. Techxplore, 2025/10/3
--------------------------------------------------------------------------------------------------------------------------------------------
【聲明】
1.科技產業資訊室刊載此文不代表同意其說法或描述,僅為提供更多訊息,也不構成任何投資建議。
2.著作權所有,非經本網站書面授權同意不得將本文以任何形式修改、複製、儲存、傳播或轉載,本中心保留一切法律追訴權利。
|